解决了百年历史的科学辩论:麻醉对意识的影响得到解决
科学家发现,台球状的细胞膜结构破裂触发了大脑因麻醉而失去知觉。
如果没有全身麻醉,手术将是不可想象的,因此,尽管有175年的医疗使用历史,但医生和科学家仍无法解释麻醉药如何使患者暂时失去知觉,这可能令人感到意外。
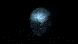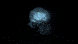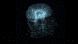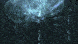
斯克里普斯研究公司(Scripps Research)的一项新研究于周四晚上在《美国国家科学院院刊》(PNAS)上发表,解决了这一长期存在的医学难题。利用现代的纳米级显微技术,再加上在活细胞和果蝇中进行的巧妙实验,科学家们证明了细胞膜中的脂质簇是如何在两部分机制之间相互缺失的。暂时暴露于麻醉状态会导致脂质团簇从有序状态转变为无序状态,然后再返回,从而导致大量后续影响,最终导致意识改变。
化学家理查德·勒纳(Richard Lerner)博士和分子生物学家斯科特·汉森(Scott Hansen)博士的发现解决了一个世纪以来的科学辩论,至今仍在酝酿:麻醉剂是否直接作用于称为离子通道的细胞膜门上,或者它们以某种新的出乎意料的方式作用于膜上,以信号通知细胞变化?二人说,经过了近五年的实验,呼吁,辩论和挑战,得出的结论是这是一个两步过程,始于膜。麻醉剂扰乱了被称为“脂质筏”的细胞膜内的有序脂质簇,从而引发了信号。

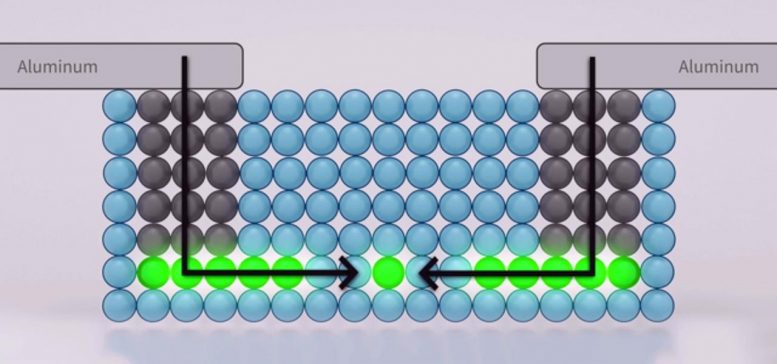
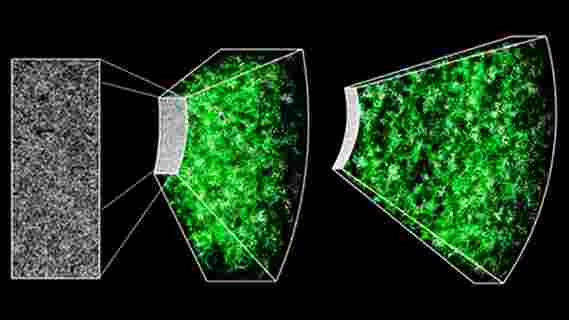
暴露于氯仿时,细胞膜中有序的胆固醇簇会暂时变得混乱。
勒纳说:“我们认为这一新颖的途径毫无疑问会被用于意识以外的其他大脑功能,这使我们现在能够消除大脑的其他谜团。”
勒纳(Lerner)是美国国家科学院的成员,曾担任斯克里普斯研究中心(Scripps Research)的总裁,也是斯克里普斯研究中心(Scripps Research)位于佛罗里达州朱庇特(Jupiter)的创始人。汉森(Hansen)是他在同一校园里的第一篇副教授。
醚穹顶
1846年,在波士顿麻萨诸塞州综合医院的一名肿瘤患者中,首先在外科手术室(后来被称为“以太穹顶”)中证明了以太尔引起意识丧失的能力。结果如此重要,以至于罗伯特·C·欣克利(Robert C. Hinckley)在著名的画作《以太下的第一行动》中捕捉到了这一过程。到1899年,德国药理学家汉斯·霍斯特·迈耶(Hans Horst Meyer),然后在1901年,英国生物学家查尔斯·欧内斯特·奥弗顿(Charles Ernest Overton)明智地得出结论,脂溶性决定了这种麻醉药的效力。
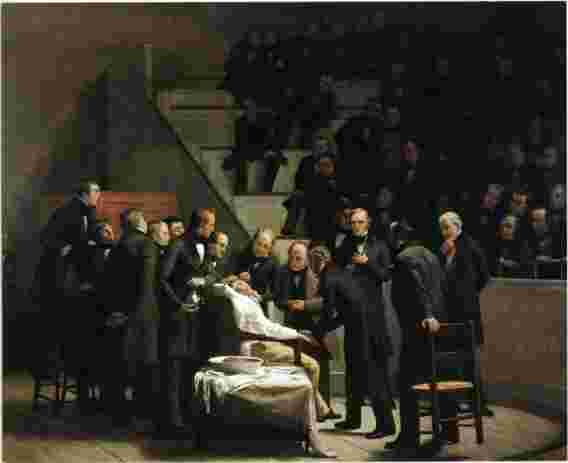
全身麻醉已经使用了将近175年,但至今尚不清楚其引起意识丧失的机制。罗伯特·辛格利(Robert C. Hinckley)在这幅画作《以太的第一个行动》中纪念了以太坊的首次使用。
汉森(Hansen)回忆起起草Google资助申请书时起草了一份赠款,以进一步调查这个历史性问题,并认为他不可能是唯一一个相信膜脂筏作用的人。令汉森高兴的是,他从勒纳(Lerner)1997年的PNAS论文“关于全身麻醉的内源性类似物的假设”中找到了一个p,提出了这样一种机制。汉森长久以来一直仰望勒纳-从字面上看。汉森说,作为圣地亚哥的博士前学生,他在地下室的实验室里工作,窗户的窗户直望斯克里普斯研究中心(Scripps Research)的勒纳(Lerner)停车位。
“我联系了他,然后我说,‘你永远不会相信这一点。您在1997年发表的p文章直观地描述了我现在在数据中看到的内容,”“汉森回忆道。“那真是太棒了。”
对于勒纳来说,这也是一个激动人心的时刻。
勒纳说:“这是医学奥秘的祖父。”“当我在斯坦福大学医学院时,这就是我要解决的问题。麻醉如此重要,我不敢相信我们不知道所有这些麻醉剂如何导致人们失去知觉。”
汉森说,许多其他科学家经过一个世纪的实验,一直寻求相同的答案,但是他们缺少几个关键要素:首先,显微镜能够可视化小于光的衍射极限的生物复合物,其次,关于细胞膜的性质以及构成它们的多种脂质复合物的复杂组织和功能的最新见解。
汉森说:“他们一直在寻找脂质的整个海洋,但信号却被冲洗掉了,他们只是看不到它,这在很大程度上是因为缺乏技术。”
从无序到无序
使用获得诺贝尔奖的显微镜技术,特别是称为“直接随机光学重建显微镜”的dSTORM显微镜,汉森实验室的一名博士后研究员将细胞浸入氯仿中,并观看了诸如打台球游戏的开裂镜头等内容。 。汉森解释说,将细胞暴露于氯仿中会大大增加称为GM1的细胞膜脂质簇的直径和面积。
汉森说,他所看到的是GM1集群组织的转变,从紧凑的球到混乱的混乱。随着无序生长,GM1溢出了其内容物,其中包括一种称为磷脂酶D2(PLD2)的酶。
Hansen用荧光化学物质标记了PLD2,通过dSTORM显微镜可以观察到PLD2像一个台球一样从其GM1家移到另一个名为PIP2的,不太受欢迎的脂质簇上。这种激活的关键分子在PIP2内成簇,其中包括TREK1钾离子通道及其脂质激活剂磷脂酸(PA)。汉森说,TREK1的激活基本上冻结了神经元的发射能力,从而导致意识丧失。
汉森说:“ TREK1钾离子通道释放钾离子,使神经超极化-使其发射起来更加困难-并将其关闭。”
Lerner坚称他们在活体动物模型中验证了发现。常见的果蝇果蝇(果蝇)提供了这些数据。删除果蝇中的PLD表达可使其抵抗镇静作用。实际上,他们需要将麻醉剂的暴露量加倍才能显示出相同的反应。
他们写道:“所有苍蝇最终都会失去知觉,这表明PLD有助于设定阈值,但不是控制麻醉敏感性的唯一途径。”
汉森(Hansen)和勒纳(Lerner)说,这些发现提出了许多诱人的新可能性,这些新可能解释了大脑的其他奥秘,包括导致我们入睡的分子事件。
勒纳(Lerner)最初于1997年提出“脂质基质”在信号传导中作用的假设,是由于他对睡眠的生物化学的研究以及他发现的一种叫做“油酰胺”的有孔脂质的发现而产生的。Hansen和Lerner在此领域的合作仍在继续。
汉森说:“我们认为这是基础和基础,但是还有很多工作要做,而且这需要很多人来完成。”勒纳同意。
“人们将开始为您能想到的一切研究这项技术:睡眠,意识,所有这些相关疾病。”他说。“醚是一种礼物,可以帮助我们理解意识问题。它揭示了迄今为止尚未被人们认识到的途径,即大脑已经明显进化为控制高阶功能。”
论文“关于全身麻醉机制的研究”发表在2020年5月29日的PNAS上。除了Lerner和Hansen,作者还有Scripps Research的Mahmud Arif Pavel,E。Nicholas Petersen和Wang Hao。
参考:Mahmud Arif Pavel,E。Nicholas Petersen,Hao Wang,Richard A.Lerner和Scott B.Hansen的“关于全身麻醉机制的研究”,2020年5月28日,美国国家科学院院刊。DOI:
10.1073 / pnas.2004259117
-
出生时的脂肪和胆固醇水平与5岁时的心理问题相关联
2022-03-23 -
现在可以监测到个体肝细胞的脂肪代谢
2022-03-11 -
新研究揭示为什么人们在变大时获得体重[视频]
2022-03-01 -
分子开关用作癌症和糖尿病疗法的新目标点
2022-02-16 -
科学家们创造了一只吃脂肪但不会产生肥胖,对肥胖的可能治疗的老鼠
2022-02-12 -
脂肪细胞填充,酮饮食和生物化学史
2022-02-03 -
耶鲁科学家揭示了骨髓瘤的潜在原因
2021-11-23 -
Scripps研究人员开发了增强生物燃料生产的新方法
2021-09-19 -
灭活AGPS酶降低肿瘤生长,抑制癌细胞
2021-09-13 -
工程师将酵母细胞转化为生物燃料
2021-09-11 -
Croda完成对美国生命科学公司的收购
2021-07-30 -
Croda收购美国生命科学公司
2021-07-29