麻省理工学院的生物学家揭示了lncRNA如何帮助控制细胞命运
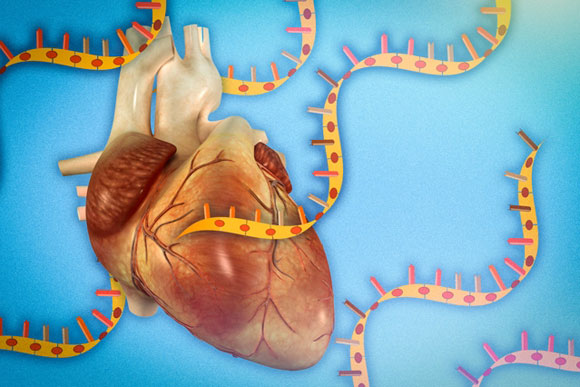
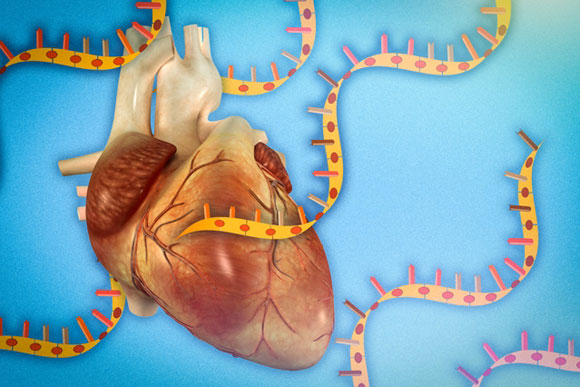
一项新的研究详细介绍了麻省理工学院的生物学家如何破译一种类型的长非编码RNA的结构,并利用该信息指出其如何与细胞蛋白相互作用以控制心肌细胞的发育。
几年前,生物学家发现了一种新型的遗传物质,称为长非编码RNA。这种RNA不编码蛋白质,而是从曾经被认为是“垃圾DNA”的基因组部分复制而来。
从那时起,科学家发现了证据,即长非编码RNA或lncRNA在许多细胞过程中发挥着作用,包括在胚胎发育过程中指导细胞命运。然而,确切地未知lncRNA如何发挥这种影响。
麻省理工学院的生物学家受到历史研究的启发,该研究表明结构在其他类别的RNA(例如转移RNA)的功能中发挥了作用,如今,麻省理工学院的生物学家已经破译了一种lncRNA的结构,并利用该信息揭示了其与细胞蛋白相互作用的方式。控制心肌细胞的发育。这是将lncRNA的结构与其功能联系起来的第一项研究之一。
“新兴数据指出了许多这些分子在发育和疾病中的基本作用,因此我们认为确定lncRNA的结构对于理解它们的功能至关重要,”欧文和海伦·塞泽尔职业发展生物学副教授Laurie Boyer说。麻省理工学院的生物工程学和该研究的资深作者,该研究发表在《分子细胞》杂志上。
了解有关lncRNA如何控制细胞分化的更多信息,可以为针对因心血管疾病,衰老或癌症而受到心脏损害的患者提供新的药物开发方法。
该论文的主要作者是麻省理工学院的博士后薛志宏。麻省理工学院的其他作者是大学本科生Boryana Doyle和Sarnoff研究员Arune Gulati。洛斯阿拉莫斯国家实验室的斯科特·汉纳利,伊琳娜·诺维科娃和卡里萨·桑邦松也都是该论文的作者。
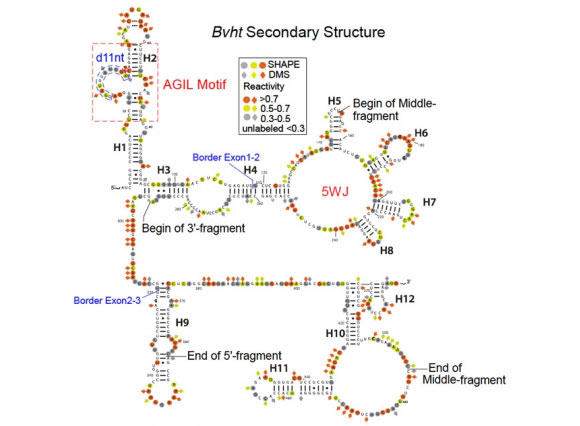
麻省理工学院的生物学家已经破译了一个名为Braveheart的长非编码RNA的结构。他们发现,左上角的AGIL基序对分子的功能至关重要。
探寻心脏
博耶实验室之前曾鉴定出一种名为“勇敢的心脏”的小鼠lncRNA,与其他组织相比,它在心脏中的含量更高。2013年,博耶(Boyer)表明,这种RNA分子对于心肌细胞的正常发育是必需的。
在这项新研究中,研究人员决定研究600个核苷酸的RNA分子的哪些区域对其功能至关重要。“我们知道《勇敢的心》对于心肌细胞的发育至关重要,但是我们不知道这种lncRNA的功能的详细分子机制,因此我们假设确定其结构可以揭示新的线索,”薛说。
为了确定《勇敢的心》的结构,研究人员使用了一种称为化学探测的技术,该技术中,他们用修饰暴露的RNA核苷酸的化学试剂处理了RNA分子。通过分析哪些核苷酸与该试剂结合,研究人员可以识别单链区域,双链螺旋,环和其他结构。
该分析表明,《勇敢的心》具有几个不同的结构区域或图案。然后研究人员测试了这些基序中的哪一个对分子的功能最重要。令他们惊讶的是,他们发现去除11个核苷酸(构成仅占整个分子2%的环)可以阻止正常的心脏细胞发育。
然后,研究人员搜索了“勇敢之心”环可能与之相互作用以控制心脏细胞发育的蛋白质。在大约10,000种蛋白质的筛选中,他们发现称为细胞核酸结合蛋白(CNBP)的转录因子蛋白质与该区域牢固结合。先前的研究表明,CNBP中的突变可导致小鼠和人类的心脏缺陷。
进一步的研究表明,CNBP可能成为心脏发育的潜在障碍,而《勇敢的心》会释放这种阻遏物,从而使细胞成为心肌。
哈佛大学干细胞与再生生物学教授约翰·里恩(John Rinn)说:“这是将lncRNA的结构与功能联系起来的第一批研究之一。”
“至关重要的是,如果我们要使lncRNA与蛋白质同步发展,那么我们必须了解特定的功能域及其结构元素,而在蛋白质中我们已经知道某些部分如何发挥特定的作用。”实际上,由于已知蛋白质具有丰富的结构与功能关系,因此您可以预测当今蛋白质的功能。 Rinn说。
建立指纹
科学家尚未鉴定出人类与小鼠勇敢者lncRNA对应的人类,部分是因为人类和小鼠lncRNA序列的保守性很差,尽管这两个物种的蛋白质编码基因通常非常相似。但是,既然研究人员知道小鼠勇敢者lncRNA的结构,他们计划分析人lncRNA分子以鉴定相似的结构,这表明它们具有相似的功能。
博耶说:“我们正在使用这个基序,并且正在使用它来构建指纹,以便我们有可能找到跨物种的类似于lncRNA的基序。”“我们还希望将这项工作扩展到识别基序目录的作用方式,以便我们可以更好地预测具有重要功能的lncRNA。”
研究人员还计划将他们对lncRNA的了解应用于工程新疗法。博耶说:“我们完全希望,揭开lncRNA的结构与功能之间的关系,将在不久的将来开辟令人振奋的新疗法。”
出版物:薛志红等,“ lncRNA Braveheart中的G富基序与锌指转录因子相互作用以指定心血管谱系,” Molecular Cell,2016年; doi:10.1016 / j.molcel.2016.08.010
-
新的研究提高了我们对细胞间通信的理解
2021-12-12 -
耶鲁大学的科学家重新编码生物以抵抗病毒污染
2021-12-11 -
工程师设计了针对埃博拉和H1N1流感的可编程RNA疫苗
2021-12-10 -
新传感器允许研究人员在大脑中跟踪多巴胺
2021-12-10 -
研究人员鉴定了人类鸡蛋老化的分子途径
2021-12-10 -
新材料提供弹性的“第二个皮肤”
2021-12-10 -
麻省理工学院生物学工程师计划人类细胞在其DNA中储存复杂的历史
2021-12-10 -
麻省理工学院的Alcator C-Mod Tokamak核融合反应堆套世界纪录
2021-12-06 -
麻省理工学院化学家揭示了可产生可生物降解塑料的细菌酶
2021-12-05 -
麻省理工学院工程师创建合成细胞以隔离遗传电路
2021-12-04 -
科学家们展示了如何相互安排突触
2021-12-04 -
科学家们展示了如何相互安排突触
2021-12-04 -
麻省理工学院工程师设计透明,基于凝胶的机器人
2021-12-04 -
科学家们展示了如何相互安排突触
2021-12-04 -
新的“变形”翼可以实现更高效的飞机飞行
2021-12-03